Mehr Synthesegas aus Kohlendioxid
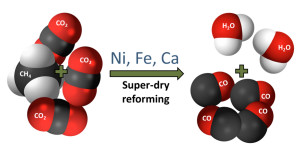
„Verglichen mit vorhandenen Technologien kann mit unserem Verfahren dreimal mehr Kohlendioxid in Kohlenmonoxid umgewandelt werden“, sagt Valdimir Galvita von der Universität Gent in Belgien. Mit seinen Kollegen optimierte er die sogenannte Trockenreformierung, bei der aus Methan (CH4)– dem Hauptbestandteil von Erdgas – und Kohlendioxid das begehrte Synthesegas entsteht. Bisher konnten in einer Katalysereaktion aus je einem CH4- und CO2-Molekül jeweils zwei Wasserstoff- und zwei Kohlenmonoxidmoleküle gewonnen werden. In dem neu entwickelten Prozess ließen sich dagegen aus drei CO2-Molekülen und einem CH4-Molekül vier Kohlenmonoxidmoleküle gewinnen. Der Wasserstoff wurde dabei in Wassermolekülen gebunden.
Möglich wurde diese signifikante Effizienzsteigerung mit einem mehrstufigen Prozess, bei dem die Forscher neben einem Katalysator aus Nickel kleine Partikel aus Eisenoxid und Calciumoxid einsetzten. Bei hohen Temperaturen von mindestens 750 Grad Celsius reagierten – unterstützt durch den Nickelkatalysator – je ein Molekül CH4 und CO2 erst zu zwei Molekülen Wasserstoff und zwei Kohlenmonoxidmolekülen. In einer darauf folgenden Redoxreaktion an Eisen- und Calciumoxid konnten noch zwei weitere CO2-Moleküle zu Kohlenmonoxid reduziert werden.
Diese Katalysereaktion hat ein großes Potenzial, die wirtschaftliche Nutzung des Treibhausgases Kohlendioxid weiter voranzutreiben. Mit dem günstigen Metall Nickel als Katalysator kann zudem auf den Einsatz teurer Edelmetalle verzichtet werden. In weiteren Arbeitsschritten muss nun überprüft werden, ob dieser Prozess auch im größeren Maßstab mit möglichst hoher Effizienz ablaufen kann. Danach könnte eine Pilotanlage für die Produktion von Synthesegas aus Kohlendioxid entstehen.

 Was Sie schon immer über Mikroben wissen wollten
Was Sie schon immer über Mikroben wissen wollten Energiewende: Schluss mit Schwarz-Weiß-Strategien
Energiewende: Schluss mit Schwarz-Weiß-Strategien Nicole Bender und Lotte Habermann-Horstmeier: Evolution und Gesundheit
Nicole Bender und Lotte Habermann-Horstmeier: Evolution und Gesundheit 