Arthrosetherapie: Nanopartikel bahnen den Weg
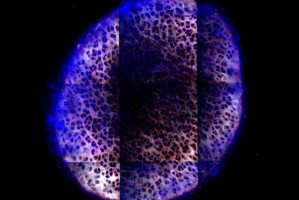
„Wir haben einen Weg gefunden, die geschädigten Knorpelzellen direkt zu erreichen. Jetzt können wir unterschiedliche Substanzen einsetzen, die auf diese Zellen einwirken“, sagt Paula Hammond vom Massachusetts Institute of Technology in Cambridge. Da der Knorpel nicht von Blutgefäßen durchzogen ist, können injizierte Wirkstoffe nur durch Diffusion in das Gewebe eindringen. Dabei haben kleine Moleküle mit positiven Ladungen einen Vorteil, da sie von den negativen Ladungen der Knorpelmatrix angezogen werden. Die Forscher synthetisierten daher eine Substanz mit diesen Eigenschaften aus der Stoffklasse der Dendrimere, die sich mit einem therapeutischen Wirkstoff verbinden und diesen in das Knorpelgewebe transportieren kann.
Die baumartig verzweigten Makromoleküle aus Polyamidoamin bildeten Nanopartikel mit einem Durchmesser von weniger als zehn Nanometern. Zur Vermeidung schädlicher Nebenwirkungen wurden die zahlreichen positiven Ladungen auf der Oberfläche teilweise durch Polyethylenglycol abgeblockt. An diese Partikel koppelten die Wissenschaftler den Wachstumsfaktor IGF-1, der Knorpelzellen schützt, ihre Vermehrung fördert und entzündungshemmend wirkt. In dieser Form in das Kniegelenk von Ratten injiziert, blieb der Wachstumsfaktor zehnmal länger im Knorpelgewebe als nach Injektion des ungebundenen Wirkstoffs. Die Halbwertszeit von freiem, ins Gelenk injiziertem IGF-1 betrug zehn Stunden. Mit der Trägersubstanz verlängerte sich diese auf bis zu vier Tage. Freies IGF-1 erreiche nur ein bis zwei Prozent des menschlichen Knorpelgewebes und dringe nur etwa 0,02 Millimeter tief ein, schreiben die Forscher. In Versuchen mit Gelenksknorpel von Kühen drang der an die Nanopartikel gebundene Wachstumsfaktor etwa einen Millimeter in das Gewebe ein. Um alle Knorpelzellen im Gelenk eines Menschen zu erreichen, müssten ein bis zwei Millimeter durchdrungen werden.
Bei Ratten verringerte eine einmalige Injektion von trägergebundenem IGF-1 die Knorpelschäden einer Kniegelenksarthrose in vier Wochen um 60 Prozent. Dabei traten keine Gewebeschäden in Leber, Nieren und Lungen auf. Da die Knorpelschicht bei Ratten etwa zehnmal dünner ist als beim Menschen, sollen zunächst Experimente mit Kühen zeigen, ob ein vergleichbarer Therapieerfolg auch bei größerer Schichtdicke des Gelenksknorpels erreichbar ist. Wenn auch klinische Studien erfolgreich verlaufen, wären Behandlungen durch monatliche Injektionen in die erkrankten Gelenke möglich, vermuten die Autoren. Anstelle von IGF-1 könnten auch andere Wirkstoffe an die Nanopartikel gebunden werden und so die Therapie weiter verbessern.

 Was Sie schon immer über Mikroben wissen wollten
Was Sie schon immer über Mikroben wissen wollten Energiewende: Schluss mit Schwarz-Weiß-Strategien
Energiewende: Schluss mit Schwarz-Weiß-Strategien Nicole Bender und Lotte Habermann-Horstmeier: Evolution und Gesundheit
Nicole Bender und Lotte Habermann-Horstmeier: Evolution und Gesundheit 