Stammzelltherapie mit iPS-Zellen: Das Immunsystem spielt nicht mit
"Dieses Ergebnis bedeutet nicht, dass man keine iPS-Zellen für klinische Zwecke verwenden darf", sagt Yang Xu von der University of California in San Diego, der Leiter des Forscherteams. Man müsse aber die Zellen vorher daraufhin testen, ob sie Abstoßungsreaktionen auslösen. Außerdem sei es notwendig, die Herstellungsmethode für iPS-Zellen zu verbessern, damit sie diesen Test bestehen. Zellen, die sich aus menschlichen embryonalen Stammzellen entwickeln, werden vom Immunsystem immer als fremd erkannt, da deren Erbgut nicht mit dem des Empfängers übereinstimmt. Wenn solche Zellen zur Therapie eingesetzt würden, wären - wie nach einer Organtransplantation - Medikamente nötig, die Abstoßungsreaktionen unterdrücken. iPS-Zellen können durch genetische Reprogrammierung von Hautzellen des Patienten erzeugt werden. In diesem Fall wären Spender und Empfänger identisch. Ob aber das Immunsystem das Gewebe, das aus übertragenen iPS-Zellen entsteht, tatsächlich als körpereigene Zellen erkennt, wurde zwar allgemein angenommen aber nie überprüft.
Immunsystem unterscheidet zwischen beiden Stammzelltypen
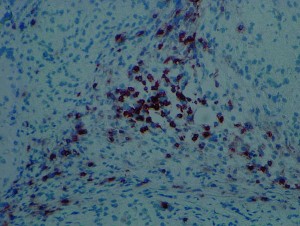
Die Forscher erzeugten sowohl embryonale Stammzellen als auch iPS-Zellen von Mäusen, die nach Inzucht genetisch weitgehend identisch waren. Unter die Haut dieser Tiere injiziert, entwickelten sich beide Stammzelltypen zu Geschwulsten, sogenannten Teratomen. Diese Gewebe bestehen aus verschiedenen Zellarten. Die aus den embryonalen Stammzellen entstandenen Teratome wurden toleriert, da sie genetisch mit den Empfängern gut übereinstimmten. Die iPS-Zell-Teratome lösten dagegen in den meisten Fällen eine Immunreaktion aus und lockten Immunzellen an, die das Gewebe angriffen.
Zwar waren die Gene beider Stammzelltypen gleich, sie unterschieden sich aber in ihren Aktivitäten. Aus den iPS-Zellen hatten sich einige Zellen entwickelt, die bestimmte Proteine im Übermaß produzierten und wahrscheinlich dadurch die Abstoßung bewirkten. Daher müsste das Herstellungsverfahren der iPS-Zellen so optimiert werden, dass sie ein normales Muster der Genaktivitäten aufweisen. Erst wenn das sichergestellt ist, so die Forscher, könnten klinische Studien zum therapeutischen Einsatz beginnen.

 Was Sie schon immer über Mikroben wissen wollten
Was Sie schon immer über Mikroben wissen wollten Energiewende: Schluss mit Schwarz-Weiß-Strategien
Energiewende: Schluss mit Schwarz-Weiß-Strategien Nicole Bender und Lotte Habermann-Horstmeier: Evolution und Gesundheit
Nicole Bender und Lotte Habermann-Horstmeier: Evolution und Gesundheit 