Neuer Ansatz für Parkinson-Therapie: Hirnzellen regeneriert
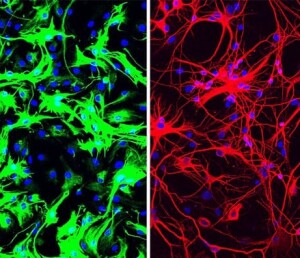
„Wir waren sehr überrascht, dass wir auf relativ einfache Weise so viele Neuronen produzieren können“, sagt Xiang-Dong Fu von der University of California San Diego. Frühere Versuche anderer Forscher, mit Hilfe von Stammzellen Neuronen zu erzeugen und geschädigtes Hirngewebe zu regenerieren, waren nur wenig erfolgreich. Fu und seine Kollegen hatten zufällig entdeckt, dass sich Bindegewebszellen und andere Typen von Mauszellen zu Nervenzellen entwickeln, wenn ein bestimmtes Gen ausgeschaltet wird. Dieses Gen trägt die Information für die Produktion des Proteins PTB, das sich an RNA-Moleküle anlagert und dadurch Gene aktivieren oder inaktivieren kann. Eine Strategie zur gezielten Eliminierung von PTB könnte geeignet sein, um abgestorbene Hirnzellen zu ersetzen.
Als Versuchstiere dienten Mäuse, deren dopaminbildende Neuronen durch eine spezielle chemische Behandlung zerstört wurden. Der so erzeugte Dopaminmangel verursachte Bewegungsstörungen, wie verlangsamte Bewegungen, Zittern und unsicherer Gang, die auch für Parkinsonpatienten typisch sind. Zunächst gingen die Forscher von Zellkulturen aus, in denen sie Astrozyten von Mäusen oder Menschen anzüchteten. Durch Zugabe gentechnisch veränderter Viren übertrugen sie in die Zellen DNA-Moleküle, aus denen dann RNA-Moleküle entstanden, die das PTB-Gen blockierten. Das aktivierte mehrere für Neuronen typische Gene und inaktivierte Astrozyten-Gene. In Versuchen mit Mäusen ist es anschließend gelungen, auch durch direkte Injektion so genannter Antisense-Oligonukleotide eine vorübergehende Blockade des PTB-Gens zu bewirken. Die Behandlung erhöhte nach zwölf Wochen die Zahl an Neuronen im Mittelhirn um etwa 30 Prozent.
Die erzeugten Neuronen produzierten Dopamin und bildeten Fortsätze, die Verbindungen zu anderen Nervenzellen herstellten. Der Dopaminspiegel im Mittelhirn stieg auf normale Werte an, so dass die Tiere nach drei Monaten keine Bewegungsstörungen mehr zeigten. Eine einzige Behandlung war ausreichend für einen dauerhaften Heileffekt. Ob dieser Therapieansatz direkt auf Menschen übertragbar ist, sei noch ungewiss, sagt Fu. Zum einen entspricht die bei den Mäusen ausgelöste Erkrankung nicht ganz der Parkinson-Krankheit. Zum anderen ist noch nicht geklärt, ob sich auch Astrozyten älterer Menschen noch zu Neuronen umprogrammieren lassen und wie groß das Risiko schwerer Nebenwirkungen ist. Doch wenn sich die neue Behandlungsstrategie als geeignet erweist, so die Autoren, wären auch Therapien anderer neurodegenerativer Erkrankungen wie Alzheimer und Huntington denkbar.

 Was Sie schon immer über Mikroben wissen wollten
Was Sie schon immer über Mikroben wissen wollten Energiewende: Schluss mit Schwarz-Weiß-Strategien
Energiewende: Schluss mit Schwarz-Weiß-Strategien Nicole Bender und Lotte Habermann-Horstmeier: Evolution und Gesundheit
Nicole Bender und Lotte Habermann-Horstmeier: Evolution und Gesundheit 