Venusfliegenfalle für Nuklear-Müll
Eine Molekül-Falle kann radioaktive Stoffe in Flüssigkeit binden und macht sie so leichter handhabbar
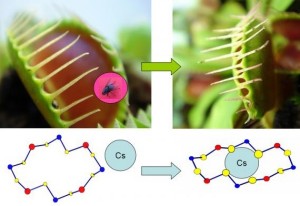
Die offenen Poren des Schichtmaterials erwarten Cäsium-Ionen wie fleischfressende Pflanzen eine Fliege. Mit Eintreffen des passenden Objektes bindet das Cäsium mit dem Sulfid im Material und die geschlossene Pore hält das Ion fest
© Mercouri Kanatzidis, Nan Ding, Northwestern
Evanston (USA) - Mülltrennung für radioaktive Flüssigkeiten soll ein neues Material aus den USA ermöglichen: Es bindet radioaktive Cäsium-Ionen, während es andere und ungefährliche im Wasser gelöste Substanzen ignoriert. Das Einfangen des Cäsiums funktioniert nach dem Prinzip einer Venusfliegenfalle. US-Forscher entwickelten das Material mit winzigen Löchern, die das Cäsium aufnehmen und dann quasi zuschnappen, weil sich mit der Bindung die Formstruktur verändert. Damit würden die radioaktiven Ionen zwar nicht vernichtet, doch so isoliert, dass sie sich gezielter transportieren und entsorgen lassen. Andernfalls müsste die gesamte Flüssigkeitsmenge entsorgt werden, obwohl das radioaktive Cäsium oft nur etwa ein Tausendstel der gelösten Ionen ausmacht. Doch ein Einsatz in der Atommülltrennung ist nicht das einzig Interessante am Material. Die Forscher sehen darin auch wichtige neue Erkenntnisse, um andere neue Materialien zum gezielten Einfangen schwer fassbarer Ionen zu entwickeln.
"Die Größe, Form und Flexibilität der Löcher erlaubt Cäsium-Ionen in einer wässrigen Lösung, gezielt zu passieren und in das Material per Ionenaustausch-Prozess hineinzukommen", schreiben Mercouri Kanatzidis und Nan Ding von der Northwestern University im Fachblatt "Nature Chemistry". Die Materialforscher entwickelten ein geschichtetes Material unter anderem aus Gallium, Schwefel und Antimon, welches mit Poren versehen ist. Im Grundzustand misst deren Öffnung 0,3 mal 0,8 Nanometer, so dass ein Cäsium-Ion gerade hinein passt. Im Inneren der Höhle geht das Cäsium mit dortigen Sulfid-Ionen eine schwache Bindung ein, was die Form des Materials verändert. Die Öffnung schließt sich und das Cäsium ist gefangen. Andere eventuell im Wasser gelöste Ionen, etwa Natrium im Salzwasser, sind so von Wassermolekülen umgeben, dass sie diese Veränderung nicht auslösen können.
(c) Wissenschaft aktuell
Quelle: "Selective incarceration of caesium ions by Venus flytrap action of a flexible framework sulfide", Nan Ding & Mercouri G. Kanatzidis; Nature Chemistry , Online-Vorabveröffentlichung. doi:10.1038/nchem.519


 Was Sie schon immer über Mikroben wissen wollten
Was Sie schon immer über Mikroben wissen wollten Energiewende: Schluss mit Schwarz-Weiß-Strategien
Energiewende: Schluss mit Schwarz-Weiß-Strategien Nicole Bender und Lotte Habermann-Horstmeier: Evolution und Gesundheit
Nicole Bender und Lotte Habermann-Horstmeier: Evolution und Gesundheit 