Warum fettreiche Ernährung das Wachstum von Metastasen beschleunigt
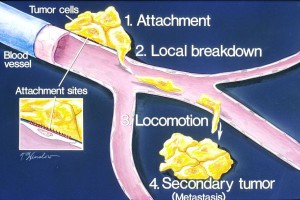
„Wir haben es zwar noch nicht für alle Tumorarten überprüft, aber wahrscheinlich ist der Rezeptor CD36 ein generelles Kennzeichen aller metastasierender Zellen“, sagt Salvador Aznar Benitah vom Institute for Research in Biomedicine in Barcelona, der Leiter der Arbeitsgruppe. Die Forscher arbeiteten zunächst mit Zellen menschlicher Mundtumoren, die sie in die Mundhöhle von Mäusen injizierten. Die Zellen, die sich zu Tumoren weiterentwickelten, produzierten große Mengen des Membranproteins CD36, das als Rezeptor für Fettsäuren dient. Auch mehrere Gene, die die Verwertung von Fettsäuren steuern, waren in diesen Zellen besonders stark aktiviert. Verglichen mit normal gefütterten Tieren, entwickelten sich bei Mäusen, die mit fettreicher Kost ernährt wurden, die injizierten Mundkrebszellen mit mehr als doppelt so großer Wahrscheinlichkeit zu Metastasen. Auch Zahl und Größe der Tumoren waren erhöht. Eine zweitägige Vorbehandlung der Mundkrebszellen mit Palmitinsäure, einem häufigen Bestandteil von Fetten und Ölen, verdoppelte ihr Potenzial, in den Versuchstieren Metastasen zu erzeugen. Der enge Zusammenhang zwischen dem Fettgehalt der Nahrung und dem Wachstum von Metastasen müsste in weiteren Studien genauer untersucht werden, sagt Benitah.
Als die Forscher mit Hilfe eines Antikörpers die CD36-Rezeptoren der Krebszellen blockierten, verhinderte das die Fähigkeit zur Metastasenbildung vollständig, ohne dass gravierende Nebenwirkungen auftraten. Hatten sich bereits Metastasen entwickelt, bewirkte eine Behandlung mit dem Antikörper, dass die Tumoren bei 20 Prozent der Tiere ganz verschwanden und bei den übrigen um 80 bis 90 Prozent schrumpften. Auch die Zellen anderer menschlicher Krebsarten wie Melanome und Brusttumore bildeten bei Blockierung des CD36-Rezeptors deutlich weniger Metastasen. Eine Analyse von Tumorgeweben aus Patienten mit Eierstock-, Blasen- oder Lungenkrebs ergab, dass die Entwicklung von Metastasen auch in diesen Fällen mit einer verstärkten CD36-Produktion verbunden war. Sollte sich der Einsatz des Antikörpers auch in Studien am Menschen als erfolgreich erweisen, so die Autoren, dann könnte die neue Therapie in fünf bis 10 Jahren zur Verfügung stehen.

 Was Sie schon immer über Mikroben wissen wollten
Was Sie schon immer über Mikroben wissen wollten Energiewende: Schluss mit Schwarz-Weiß-Strategien
Energiewende: Schluss mit Schwarz-Weiß-Strategien Nicole Bender und Lotte Habermann-Horstmeier: Evolution und Gesundheit
Nicole Bender und Lotte Habermann-Horstmeier: Evolution und Gesundheit 