Nanostruktur menschlicher Knochen entschlüsselt
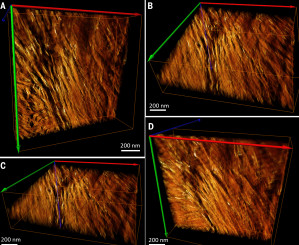
„Derzeit wird intensiv diskutiert, wie im Knochengewebe steife und flexible Phasen kombiniert werden und dem Knochen sowohl Zähigkeit als auch Festigkeit verleihen“, sagt Roland Kröger, Physikprofessor an der University of York. Diese Diskussion bereichert er nun gemeinsam mit Kollegen des Imperial College London mit extrem hochaufgelösten Bildern aus dem Innern von Oberschenkelknochen. Die Knochenproben wurden unter Beachtung strenger ethischer Standards bei Operationen von zwei Frauen im Alter von 48 und 50 Jahren gewonnen. Kröger und Kollegen benötigten für ihre Analysen nur etwa 100 Nanometer dünne Knochenschnitte. Mit ausgeklügelten bildgebenden Verfahren – der Elektronen-Tomographie und der Rasterelektronenmikroskopie gewannen sie zwei- und dreidimensionale Aufnahmen. Diese Bilder kombinierten die Forscher miteinander und erreichten so eine räumliche Bildauflösung von wenigen Nanometern.
Mit dieser Analyse erweiterten Kröger und Kollegen das aktuelle Wissen deutlich. Im Wesentlichen bilden Knochen ein Kompositmaterial aus zwei Substanzen: das flexible Strukturprotein Kollagen und die harten Kristalle des Minerals Apatit. Diese beiden Substanzen werden in einem hierarchischen Aufbau miteiander kombiniert. Knochen erreichen dadurch mechanische Eigenschaften, die besser sind als die von jeder Substanz allein. Genau diesen hierarchischen Aufbau vom Molekül bis zum Knochen als Ganzes analysierten die Wissenschaftler mit zuvor unerreichter Genauigkeit. Ihr Ergebnis: Weiches Kollagen und hartes Apatit setzt sich über insgesamt zwölf Stufen zu sich selbst ähnlichen, fraktalartigen Strukturen zusammen.
Im Detail lagern sich unterhalb von 100 Nanometern Kollagen-Moleküle zu zunehmend komplexeren, in sich gewundenen Mikrofasern zusammen. Im gleichen Größenbereich formen die Apatit-Kristalle zuerst kleine Nanoplättchen, die sich darauf zu winzigen Stapeln zusammenlagern. Auch ineinander verdrehte Stapel vergleichbar mit winzigen Propellern sind dabei möglich. Erst in der folgenden Stufe verknüpfen sich die weichen Kollagen-Fasern mit den harten, kristallinen Apatit-Stapeln zu wenige Mikrometer großen Fasern. Diese Fasern ordnen sich in teils geordneten, teils ungeordneten Strukturen zusammen, um sich dann zu größeren Faserbündeln zu verdrillen. Mehrere Faserbündel bilden geschichtete Lamellenstrukturen, die schließlich als Bausteine für wenige Millimeter große Lamellen-Pakete in der Knochenstruktur dienen.
Mit ihrer Analyse gelang Kröger und Kollegen ein verblüffender Einblick in den Aufbau von menschlichen Knochen. Damit schufen sie eine Datenbasis, um die mechanischen Eigenschaften des im Körper stets nachwachsenden Gewebes besser zu verstehen. Anwendungen könnten nicht nur im medizinischen Bereich bei der Optimierung des Knochenaufbaus von Patienten, sondern auch in der Entwicklung hochfester und zugleich flexibler bionischer Werkstoffe liegen.

 Was Sie schon immer über Mikroben wissen wollten
Was Sie schon immer über Mikroben wissen wollten Energiewende: Schluss mit Schwarz-Weiß-Strategien
Energiewende: Schluss mit Schwarz-Weiß-Strategien Nicole Bender und Lotte Habermann-Horstmeier: Evolution und Gesundheit
Nicole Bender und Lotte Habermann-Horstmeier: Evolution und Gesundheit 