Kleinste Reaktionskammer der Welt
„Wir haben gezeigt, dass eine so funktionierende Vorrichtung hergestellt werden kann und dabei in einem sehr kleinen Volumen tatsächlich biochemische Reaktionen ablaufen“, berichtet Peter Derrik, Professor für physikalische Chemie und Chemikophysik an der Massey University in Neuseeland. Gemeinsam mit britischen und österreichischen Kollegen griff er zur weit verbreiteten Elektrospray-Ionisation, wobei eine Flüssigkeit in viele kleine elektrisch geladene Tröpfchen verwandelt wird, wenn sie durch eine feine Düse geschickt wird, an welcher Hochspannung anliegt. Auch die Substanzen in der Flüssigkeit werden dabei ionisiert – in dieser elektrisch geladenen Form kann ein Massenspektrometer sie nach Ladung und Masse sortieren und damit genau identifizieren.
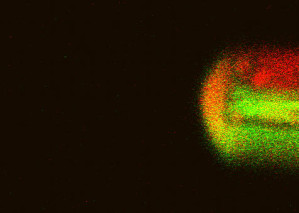
Doch während üblicherweise eine flüssige Substanz durch viele Düsen gleichzeitig gedrückt wird, kombinierte Derriks Team gleich zwei Substanzen in einem Tropfen. Direkt an der Düse bildet die elektrisch geladene Flüssigkeit – unter extremer Zeitlupe betrachtet – zunächst eine Wölbung nach außen. Dieser sogenannte Taylor-Kegel ist die Vorform des später sich ablösenden Tropfens. Doch die Forscher stellten fest: Wenn zwei feine Düsen dicht nebeneinander ihre Flüssigkeit ausstoßen, können sie einen gemeinsamen Taylor-Kegel bilden. Sind die Düsen fein genug, so enthält der dabei entstehende gemeinsame Tropfen nur wenige Femto-Liter Flüssigkeit. In seinem Inneren können die enthaltenen Moleküle miteinander reagieren. Dass tatsächlich neue chemische Verbindungen entstehen, bestätigte eine direkt anschließende Massenspektrometrie. Von der geringen Menge der Moleküle her entsprechen diese Reaktionen den Vorgängen in lebenden Zellen, so Derrik.
Für das Experiment konstruierte sein Team aus einem handelsüblichen Elektrospray-Gerät mit einzelnen runden Düsen von nur 4,5 Mikrometern Durchmesser eine Vorrichtung mit zwei halbrunden Kanälen. Tests mit verschieden gefärbten Flüssigkeiten zeigten, dass die Taylor-Kegel miteinander verschmolzen. Dann kombinierten die Forscher das Antibiotikum Vancyomycin mit einer Flüssigkeit mit den Peptiden, an die das Antibiotikum im Körper bindet. Tatsächlich enthielten die kombinierten Tropfen nach wenigen Zehntel Mikrosekunden die Moleküle, die aus Vancyomycin und Peptiden entstehen. Auch weitere Kombinationen lieferten das erwartete Ergebnis, so die Forscher. Dass sahen sie als Beleg, dass Innerhalb des winzigen Tropfens chemische Reaktionen stattfanden.

 Was Sie schon immer über Mikroben wissen wollten
Was Sie schon immer über Mikroben wissen wollten Energiewende: Schluss mit Schwarz-Weiß-Strategien
Energiewende: Schluss mit Schwarz-Weiß-Strategien Nicole Bender und Lotte Habermann-Horstmeier: Evolution und Gesundheit
Nicole Bender und Lotte Habermann-Horstmeier: Evolution und Gesundheit 